Alcohol-Distillatie
Wat is distillatie.

Distillatie is een methode voor het scheiden van mengsels op basis van verschillen in hun kookpunt, en is een fysiek scheidingsproces, en niet een chemische reactie. Commercieel kent distillatie een aantal toepassingen.
Het wordt gebruikt om olie in meer fracties om te zetten zoals ruwe olie naar gas, benzine, diesel nafta en teer. Water word gedistilleerd om verontreinigingen, zoals zout uit zeewater te verwijderen. Lucht wordt gedistilleerd om de componenten-met name zuurstof, stikstof te scheiden en argon-voor industrieel gebruik.
Distillatie van gefermenteerde (vergiste) oplossingen (stookwijn) word sinds de oudheid gebruikt om gedistilleerde dranken te produceren met een hoger alcoholgehalte. De lokalen waar de distillatie wordt uitgevoerd, met name de distillatie van alcohol, staan bekend als een distilleerderij. Voor het distilleren van alcohol gebruikt men een Labiek of stookketel met kollom. Kijk, en nu zijn we er.
Het wordt gebruikt om olie in meer fracties om te zetten zoals ruwe olie naar gas, benzine, diesel nafta en teer. Water word gedistilleerd om verontreinigingen, zoals zout uit zeewater te verwijderen. Lucht wordt gedistilleerd om de componenten-met name zuurstof, stikstof te scheiden en argon-voor industrieel gebruik.
Distillatie van gefermenteerde (vergiste) oplossingen (stookwijn) word sinds de oudheid gebruikt om gedistilleerde dranken te produceren met een hoger alcoholgehalte. De lokalen waar de distillatie wordt uitgevoerd, met name de distillatie van alcohol, staan bekend als een distilleerderij. Voor het distilleren van alcohol gebruikt men een Labiek of stookketel met kollom. Kijk, en nu zijn we er.
Het proces van alcohol distillatie.
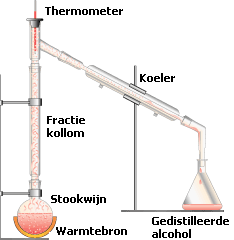
De stookwijn word verwarmd en de ethanol die een lager kookpunt heeft dan water gaat over van vloeistof naar gasvorm.
Deze stijgt op in de fractiekollom, komt langs de thermometer (waar we overigens rond de 80 graden willen aflezen) en gaat richting de koeler (productkoeler) alwaar het ethanolgas door de koelende werking word gecondenseerd en uiteindelijk word opgevangen als gedistilleerde ethanol.
Nu verwachten we 100% ethanol............niet dus.
Alhoewel het kookpunt van water op 100 graden ligt, zullen er toch bij lagere temperaturen al watermoleculen over gaan in gas (deze zijn niet al te vluchtig) en mee komen met de ethanol.
De kollom waar de gassen in opstijgen is relatief kouder en er vind enigsinds een condensatie plaats in de kollom waarbij de gecondenseerde delen weer de stookwijn in vallen en alleen de vluchtigere gassen hoger en hoger gaan in de kollom.
Om een hogere ethanolpercentage te bereiken zal er een betere scheiding moeten worden gerealiseerd, dit kan op verschillende methoden:
Rashig ringen
Als we de kollom vullen met ringen, zal er in de kollom een grotere oppervlakte gecreerd die relatief koeler is, er treed een voorcondensatie op, alleen de echt vluchtige gassen gaan nog tussen de ringen door en de laagkokende bestanddelen condenseren op het relatieve koelende oppervlak van de ringen. De gecondenseerde omlaag vallende druppels komen het omhoog stijgende gas tegen, hierdoor vind een uitwisseling plaats en deze levert een extra scheiding op, dus hogere ethanolpercentages.
De ringen worden overigens Rashigringen genoemd en zijn meestal van keramisch materiaal, maar kunnen ook van glas of rvs zijn.
Enkele amateurstokers gebruiken i.p.v. ringen ook wel rvs pannensponzen of knikkers.
Willen we een nog betere scheiding, dan kunnen we in de kollom ook nog een koeler plaatsen, de zogenaamde refluxkoeler waarbij een nog betere voorcondensatie plaatsvind. Het hoogste ethanol percentage wat men met distilleren kan halen is 96%, dit komt doordat water-ethanol een azeotroop vormt.
We hebben te maken met 2 soorten alcoholen, Methylalcohol (Methanol) en Ethylalcohol (Ethanol).
De Ethanol willen we hebben, de Methanol niet want die is giftig. Verder zijn er nog Propylalcohol, Butylalcohol, Amaylalcohol en Caprylalcohol, deze hebben een kookpunt van 96 graden en hoger tot wel 150 graden. In principe komen wij met stoken niet tot deze temperaturen en hebben hier verder geen last van.
Methanol word geproduceerd tijdens het fermenteren (vergisten) doordat de houtdelen van fruit die Pectine bevat , zoals steeltjes en pitten, worden omgezet naar Methanol. Bij consumptie hiervan word de Methanol in je lichaam omgezet naar mierezuur, die tasten uiteindelijk je zenuwen aan (de oogzenuwen zijn hier het gevoeligst voor, vandaar het alom bekende verhaal van blindheid bij zelfgemaakte drank)
Dus voor de volledige veiligheid vergisten we alleen suiker i.p.v. fruit, en is er geen kans op Methanol.
Deze stijgt op in de fractiekollom, komt langs de thermometer (waar we overigens rond de 80 graden willen aflezen) en gaat richting de koeler (productkoeler) alwaar het ethanolgas door de koelende werking word gecondenseerd en uiteindelijk word opgevangen als gedistilleerde ethanol.
Nu verwachten we 100% ethanol............niet dus.
Alhoewel het kookpunt van water op 100 graden ligt, zullen er toch bij lagere temperaturen al watermoleculen over gaan in gas (deze zijn niet al te vluchtig) en mee komen met de ethanol.
De kollom waar de gassen in opstijgen is relatief kouder en er vind enigsinds een condensatie plaats in de kollom waarbij de gecondenseerde delen weer de stookwijn in vallen en alleen de vluchtigere gassen hoger en hoger gaan in de kollom.
Om een hogere ethanolpercentage te bereiken zal er een betere scheiding moeten worden gerealiseerd, dit kan op verschillende methoden:
Rashig ringen
Als we de kollom vullen met ringen, zal er in de kollom een grotere oppervlakte gecreerd die relatief koeler is, er treed een voorcondensatie op, alleen de echt vluchtige gassen gaan nog tussen de ringen door en de laagkokende bestanddelen condenseren op het relatieve koelende oppervlak van de ringen. De gecondenseerde omlaag vallende druppels komen het omhoog stijgende gas tegen, hierdoor vind een uitwisseling plaats en deze levert een extra scheiding op, dus hogere ethanolpercentages.
De ringen worden overigens Rashigringen genoemd en zijn meestal van keramisch materiaal, maar kunnen ook van glas of rvs zijn.
Enkele amateurstokers gebruiken i.p.v. ringen ook wel rvs pannensponzen of knikkers.
Willen we een nog betere scheiding, dan kunnen we in de kollom ook nog een koeler plaatsen, de zogenaamde refluxkoeler waarbij een nog betere voorcondensatie plaatsvind. Het hoogste ethanol percentage wat men met distilleren kan halen is 96%, dit komt doordat water-ethanol een azeotroop vormt.
We hebben te maken met 2 soorten alcoholen, Methylalcohol (Methanol) en Ethylalcohol (Ethanol).
De Ethanol willen we hebben, de Methanol niet want die is giftig. Verder zijn er nog Propylalcohol, Butylalcohol, Amaylalcohol en Caprylalcohol, deze hebben een kookpunt van 96 graden en hoger tot wel 150 graden. In principe komen wij met stoken niet tot deze temperaturen en hebben hier verder geen last van.
Methanol word geproduceerd tijdens het fermenteren (vergisten) doordat de houtdelen van fruit die Pectine bevat , zoals steeltjes en pitten, worden omgezet naar Methanol. Bij consumptie hiervan word de Methanol in je lichaam omgezet naar mierezuur, die tasten uiteindelijk je zenuwen aan (de oogzenuwen zijn hier het gevoeligst voor, vandaar het alom bekende verhaal van blindheid bij zelfgemaakte drank)
Dus voor de volledige veiligheid vergisten we alleen suiker i.p.v. fruit, en is er geen kans op Methanol.
